Sirds mazspēja ar samazinātu izsviedes frakciju (HFrEF) ir galvenais sirds mazspējas veids, un Ķīnas HF pētījums parādīja, ka 42% sirds mazspēju Ķīnā ir HFrEF, lai gan ir pieejamas vairākas standarta terapeitiskās zāļu klases HFrEF ārstēšanai un ir samazinājušas risku. nāves gadījumi un zināmā mērā hospitalizācija sirds mazspējas dēļ. Tomēr pacientiem ir augsts atkārtotu sirds mazspējas pasliktināšanās gadījumu risks, mirstība joprojām ir aptuveni 25% un prognoze joprojām ir slikta. Tāpēc joprojām ir steidzami nepieciešami jauni terapeitiskie līdzekļi HFrEF ārstēšanā, un Vericiguat, jauns šķīstošs guanilāta ciklāzes (sGC) stimulators, tika pētīts VICTORIA pētījumā, lai novērtētu, vai Vericiguat varētu uzlabot pacientu ar HFrEF prognozi. Pētījums ir daudzcentru, randomizēts, paralēlu grupu, placebo kontrolēts, dubultmaskēts, uz notikumiem balstīts, III fāzes klīnisko iznākumu pētījums. Pētījums tika veikts Kanādas VIGOR centra aizgādībā sadarbībā ar Duke Clinical Research Institute, un pētījumā piedalījās 616 centri 42 valstīs un reģionos, tostarp Eiropā, Japānā, Ķīnā un ASV. Mūsu kardioloģijas nodaļa bija pagodināta piedalīties. Kopumā 5050 pacienti ar hronisku sirds mazspēju vecumā no ≥18 gadiem, NYHA II-IV klase, EF <45%, ar paaugstinātu natriurētiskā peptīda (NT-proBNP) līmeni 30 dienu laikā pirms randomizācijas un kuri bija hospitalizēti sirds mazspējas dēļ pētījumā tika iekļauti 6 mēnešu laikā pirms randomizācijas vai intravenozi ievadīti diurētiskie līdzekļi sirds mazspējas ārstēšanai 3 mēnešu laikā pirms randomizācijas, visi, kas saņem ESC, AHA/ACC un valsts/reģiona specifiskās vadlīnijas, ieteicamo aprūpes standartu. Pacienti tika randomizēti proporcijā 1:1 divās grupās un tika ievadītiVericiguat(n=2526) un placebo (n=2524) papildus standarta terapijai.
Pētījuma primārais mērķa kritērijs bija kombinētais galapunkts – kardiovaskulāra nāve vai pirmā sirds mazspējas hospitalizācija; sekundārie mērķa parametri ietvēra primārā mērķa komponentus, pirmo un turpmāko sirds mazspējas hospitalizāciju (pirmie un atkārtoti notikumi), salikto galarezultātu — visu iemeslu nāves vai sirds mazspējas hospitalizāciju un visu cēloņu nāvi. Vidēji 10,8 mēnešu novērošanas laikā Vericiguat grupā bija relatīvi par 10% mazāks primārais kardiovaskulāras nāves vai pirmās sirds mazspējas hospitalizācijas mērķa kritērijs, salīdzinot ar placebo grupu.
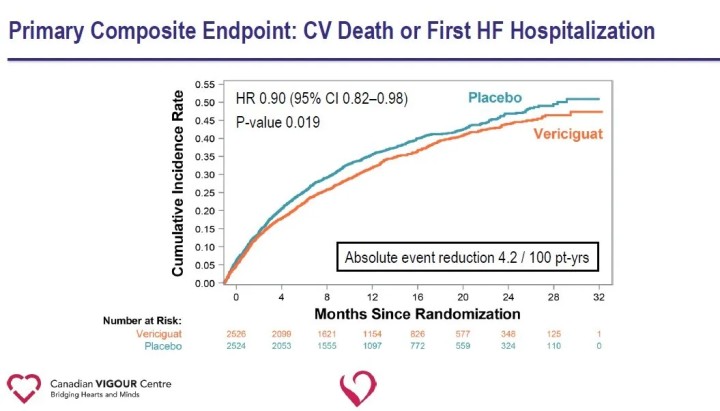
Sekundāro mērķa kritēriju analīze liecināja par nozīmīgu sirds mazspējas hospitalizācijas samazināšanos (HR 0,90) un būtisku samazinājumu kombinētajā galarezultātā saistībā ar visu iemeslu nāves vai sirds mazspējas hospitalizāciju (HR 0,90) Vericiguat grupā, salīdzinot ar placebo grupu.
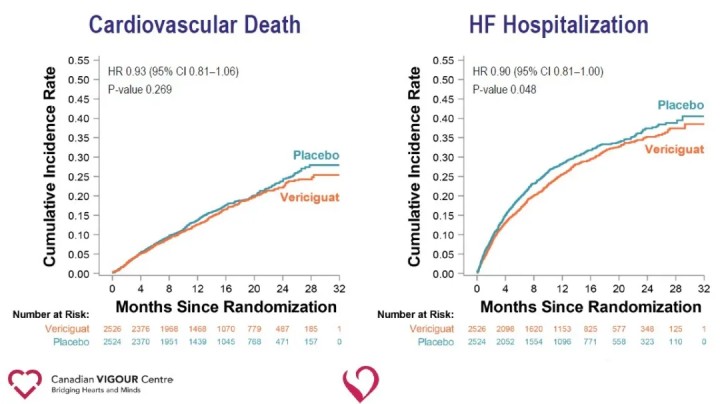
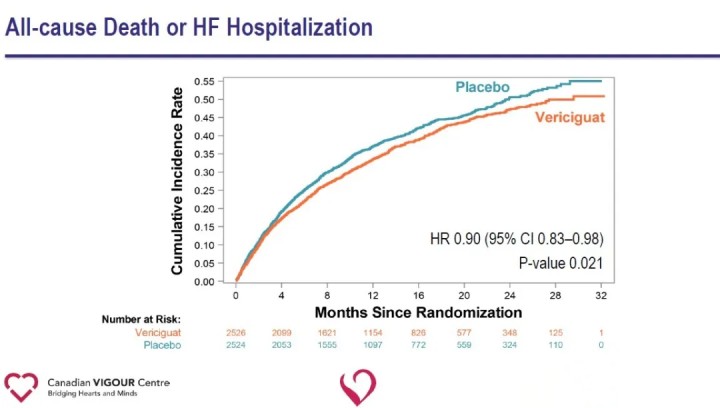
Pētījuma rezultāti liecina, ka pievienojotVericiguatStandarta sirds mazspējas ārstēšana ievērojami samazina neseno sirds mazspējas pasliktināšanās gadījumu skaitu un samazina risku, ka pacientiem ar HFrEF var rasties kardiovaskulāra nāve vai hospitalizācija sirds mazspējas dēļ. Vericiguat spēja samazināt kardiovaskulāras nāves vai sirds mazspējas hospitalizācijas saliktā mērķa risku pacientiem ar augsta riska sirds mazspēju nodrošina jaunu sirds mazspējas terapeitisko ceļu un paver jaunus ceļus turpmākai sirds un asinsvadu slimību izpētei. Vericiguat pašlaik nav apstiprināts tirdzniecībai. Zāļu drošība, efektivitāte un izmaksu lietderība tirgū joprojām ir jāpārbauda.
Publicēšanas laiks: 09.09.2022
